抗原肽组学
技术介绍
T淋巴细胞识别外源性抗原是适应性免疫的基础。多肽抗原与MHC-I和MHC-II蛋白质(major histocompatibility complex,也叫主要组织相容性复合体,如人类MHC的表达产物HLA,Human Leukocyte Antigen)结合并呈递于细胞表面,作为T淋巴细胞的作用靶点。这些多肽来源于内源性或外源性蛋白的降解。抗原处理与呈递是一个动态的过程,因蛋白的表达水平、翻译后修饰、细胞内抗原的处理活性和呈递机制等不同,呈递的免疫肽组(immunopeptidome)集合也在不断的变化。因此,细胞内各种程度的扰动会导致呈递多肽组的剧烈变化。HLAp可能来源于疾病相关抗原,并向T细胞呈递。对于设计创新的癌症治疗方法、自动免疫和抗原感染作,深入研究HLAp作用极为重要。目前,质谱是唯一的深度鉴定人细胞系、肿瘤组织和血浆等体液中HLAp的方法。前期的探索表明,基于质谱的免疫肽组学直接鉴定临床相关的新抗原(neo-antigens)已经成为可能,进而用于设计个性化的癌症疫苗。

图 1 Ⅰ类与Ⅱ类抗原呈递通路
Figure 1 Class I and Class II antigen presentation pathways
基于质谱的免疫多肽组学分析流程包含4个主要步骤:
(1) 样品制备与总蛋白提取;
(2) 免疫亲和富集(IP)HLA复合物并提取与纯化HLAp;
(3) 色谱法分离多肽并用于质谱(MS)分析;
(4) 搜库软件与生物信息学方法鉴定多肽类型。
根据该流程与新一代质谱的应用,可在每个生物学样本中鉴定到数千条HLAp。免疫肽组分析流程中最大的瓶颈在于样品制备步骤,样品的合格与否直接决定了总多肽收率和重复性。
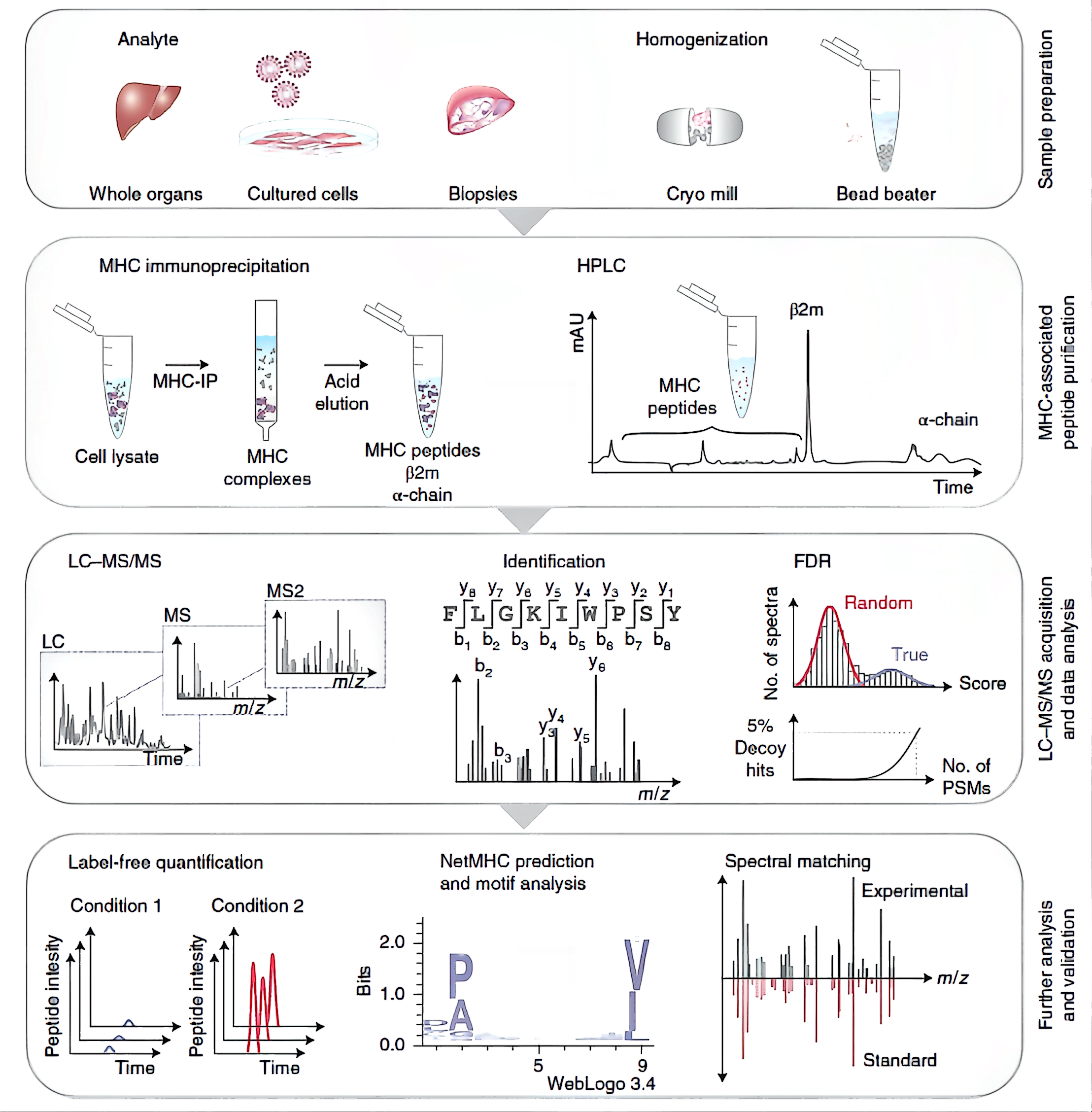
图 2 免疫多肽组学分析流程
Figure 2 Immunopeptide omics analysis process
分析仪器

Bruker timsTOF Pro2
应用范围
大于12例样品数量的大队列比较。各种细胞,亚细胞器,组织、体液(血液,尿液,唾液)发现蛋白质组研究。
样品要求
样品类型 | 样品要求(每组) |
细胞 | 细胞量>108 |
动物组织 | 新鲜组织>100 mm3 (100 mg) |
血清 | 10ml |
1. 客户需自行IP富集MHC结合的抗原肽; 2.样品溶液:请告知溶液内成分或最后一步实验所用试剂。 3.干冰运输; |
交付内容
1). 质谱原始文件; 2). 质量峰图(每个样品2张); 3). 实验方法与结果报告
参考文献
1) .Purcell, A.W., Ramarathinam, S.H. & Ternette, N. Mass spectrometry based identification of MHC-bound peptides for immunopeptidomics. Nat Protoc 14, 1687-1707 (2019).
2) .Shira W.G.,Susan, K. & Siranush, S. Profiling SARS-CoV-2 HLA-I peptidome reveals T cell epitopes from out-of-frame ORFs. Cell 184, 3962-3980 (2021).
3) .Jennife,r G. A., Dewi, H. & Matthew, M. Defining HLA-II Ligand Processing and Binding Rules with Mass Spectrometry Enhances Cancer Epitope Prediction. Immunity 51, 766-779 (2019).